米格列醇(1,miglitol)化学名为(2R,3R,4R,5S)-2-羟甲基-1-(2-羟乙基)-3,4,5-哌啶三醇,它是1-脱氧野尻霉素的衍生物,是一种强烈的α-葡萄糖苷酶抑制剂,20 世纪80 年代初由拜耳制药公司开发的抗Ⅱ型糖尿病药物,并迅速成为治疗Ⅱ型糖尿病首选药物。
目前,米格列醇的制备方法主要有两大类。一类是化学-生物转化-化学法,先经化学合成N-羟乙基葡萄糖胺中间体,然后经生物氧化转化,最后经分子内还原胺化得到米格列醇。典型合成路线如图1 所示。该方法是目前生产米格列醇最普遍的方法,但是该方法存在微生物菌培养困难,循环利用不高,产物浓度低,产量小,产物不易分离等缺点。
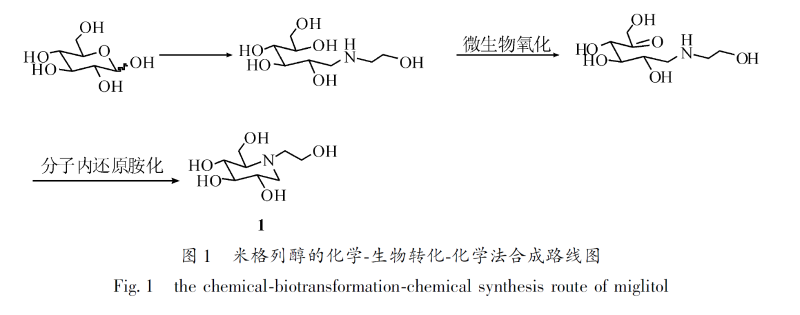
米格列醇制备的另一类方法是化学合成法,现有化学合成法普遍存在反应步骤多,产率低,立体构型难以控制,分离提纯困难等缺点。其中较有代表性的合成方法如图2 所示。
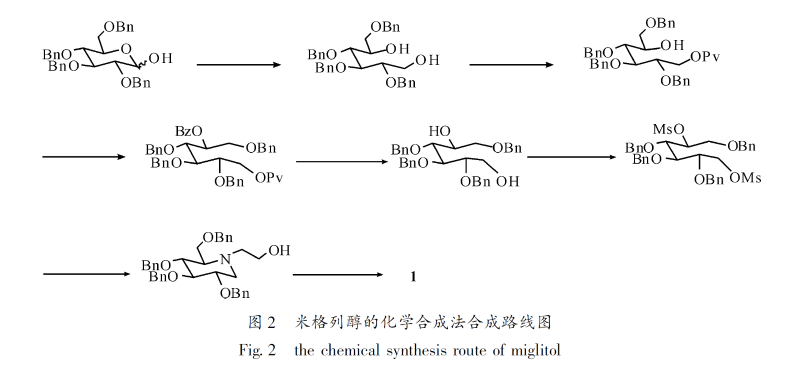
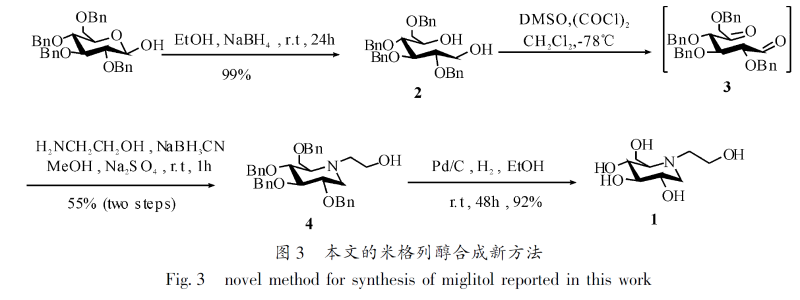
本文在总结现有化学合成方法的基础上,通过重新设计合成路线和实验研究得到了一个步骤少,操作简单,收率高的高立体选择性合成米格列醇的新方法(图3)。
1 实验部分
1. 1 主要仪器与试剂
核磁共振谱用Bruker Avance 400 型超导核磁共振仪测定, TMS 为内标; HR-ESI-MS 质谱用Bruker-maXis 质谱仪测定;比旋光度用Autopol IVT型双波长自动旋光仪(美国Rudolph 公司生产)测定;熔点用X-6 显微熔点测定仪(北京泰克仪器有限公司生产) 测定,温度未校正;HPLC 为LC-2010AHT 型高效液相色谱仪(日本岛津公司生产);PARR 5500 高压反应釜(美国)。
所用试剂均为分析纯。
1. 2 实验方法
1. 2. 1 (2,3,4,6)-O-四苄基葡糖二醇(2)的合成
在1 L 反应瓶中加入54.00 g(100 mmol)四苄基葡萄糖、硼氢化钠10.10 g(260 mmol)、500 mL 无水乙醇,室温下搅拌反应24 h,将反应液减压浓缩。给残留物中加入100.0 mL 乙酸乙酯后用水洗涤,有机相用无水Mg2SO4 干燥,过滤、浓缩后得无色透明粘稠状液体53.10 g,NMR 表征为四苄基葡萄糖二醇,HPLC 测定纯度96%,收率99%。
取四苄基米格列醇1.12 g(2 mmol)置于100 mL 高压反应釜中,加入乙醇50 mL、Pd/ C(5%)催化剂1.45 g,通入氢气至压力3 MPa 于25 ℃下搅拌反应,直至氢气压力不再下降,约需48 h。过滤,滤饼用乙醇洗涤两次,合并滤液与洗液,70℃ 真空浓缩至干,得浅黄色粘稠油状粗产物,柱色谱分离(甲醇∶氯仿= 1∶3) 得米格列醇375 mg, 收率92%, 比旋光度[α]20 D :-6.8° ( C = 0.60, H2O), 与文献报道一致。
2 结果与讨论
2. 1 合成方法的选择
本研究拟定以图3 所示的路线进行米格列醇的合成。该路线依次以2,3,4,6-O-四苄基-D-葡萄糖为原料,经硼氢化钠还原得四苄基葡萄糖二醇;利用Swern 氧化将四苄基葡萄糖二醇氧化得到四苄基葡萄糖二羰基衍生物,因该衍生物不稳定,可将其不经分离直接与乙醇胺进行双还原胺化反应关环得到四苄基米格列醇;然后在Pd/C(5%)催化剂的存在下经氢解脱苄基得到米格列醇。四步反应总收率为50%,所得产物经比旋光度测定与文献报道一致。该路线的主要优点在于对不稳定的四苄基葡萄糖二羰基衍生物不经分离直接用于下步反应,使反应副产物减少,反应收率得以提高;更重要的是所得的双还原胺化反应条件下可直接获得2-位为R 构型的光学纯目标产物。
2. 2 化合物4 制备中的立体选择性
四苄基米格列醇是该合成方法中的关键中间体,当化合物2 经Swern 氧化生成四苄基葡萄糖二羰基衍生物3 后,直接与乙醇胺进行双还原胺化时,所得化合物4 中3,4,5-三个位置的手性碳原子不是反应位点,保持其原有构型不变。在双还原胺化的过程中酮碳基接受氮原子亲核加成,再经还原后2-位新生成的手性碳可为R 构型,也可为S 构型。在本方法所述的特定条件下,双还原胺化所得产物4 经手性HPLC 测定表明其de 值为99%,高选择性地得到了所需的R 构型产物。这种高立体选择性结果可能主要是由于3,4,5-三个位置手性碳原子的不对称诱导所致。
2. 3 反应条件的优化
该研究的主要创新点在于利用乙醇胺直接与四苄基葡萄糖二羰基衍生物3 之间进行双还原胺化反应以获得四苄基米格列醇,其他各步反应在参照文献报道方法的基础上,改进而来。因此,为了提高双还原胺化反应的收率,该研究分别进行了投料比、反应温度等对反应影响的探索。在保持其他条件不变的情况下,在1 ∶2-1 ∶8摩尔比之间对反应底物(以四苄基葡萄糖二醇计)与乙醇胺的投料比进行了优化(如表1 所示)。
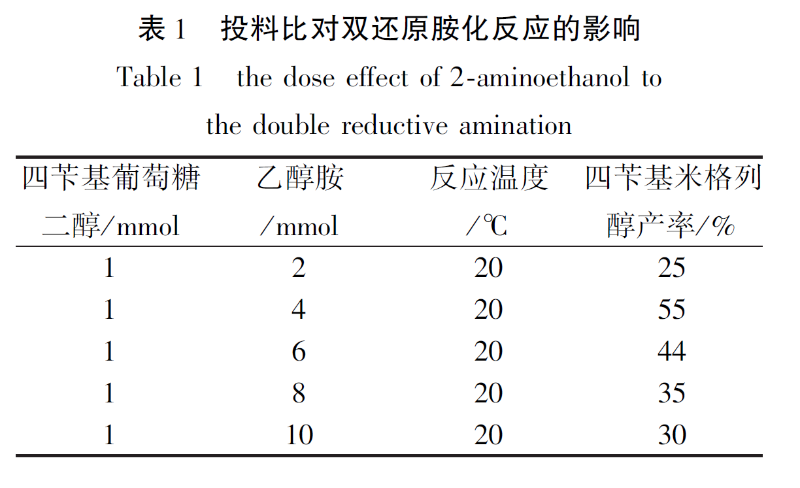
结果表明在反应时间为1 h 的情况下,当其摩尔比为1 ∶4时四苄基米格列醇的产率最高,大于1 ∶4会使产率下降,且副产物生成量增大。原因可能是大于1 ∶4时乙醇胺过量太多会使二羰基化合物的两个羰基同时与乙醇胺发生还原胺化反应,使关环环产物产率降低;小于1 ∶2时,乙醇胺浓度过小,需要更长的反应时间;由于二羰基化合物不稳定,过程中会使大量的二羰基化合物不能及时与乙醇胺反应关环,而使四苄基米格列醇产率下降。
在优化的投料比下,于20--60℃ 之间探索了温度对双还原胺化反应的影响(如表2 所示)。
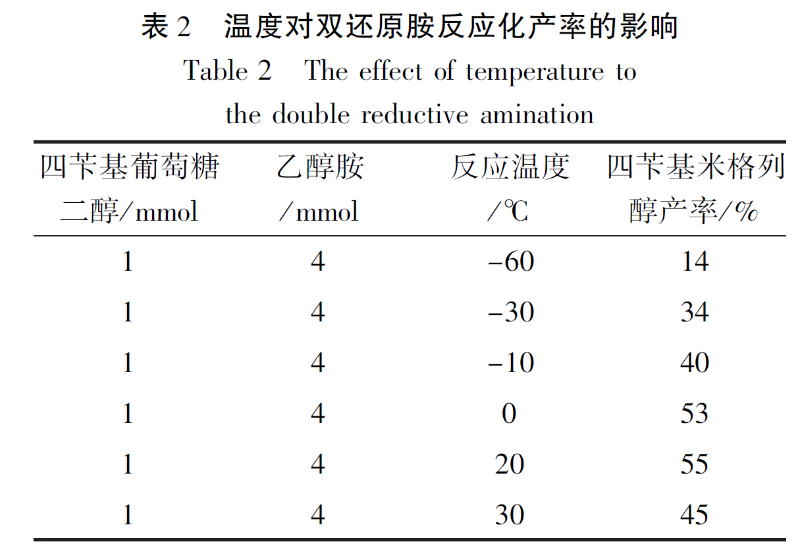
当温度在0-20℃ 时四苄基米格列醇产率较高,温度低于-10℃时,产率下降且副产物生成量增大。在优化的条件下,通过HPLC 跟踪双还原胺化反应进度,发现该反应在1h 内即可完成,延长反应时间目标产物生成量不再变化,因此确定双还原胺化反应时间为1h。
服务热线

手机联系